- Sulfure de fer(II)
-
Sulfure de fer(II) 
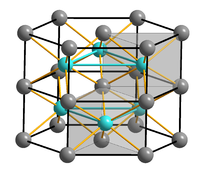
__ Fe2+ __ S2-
Structure du sulfure de fer(II)Général Nom IUPAC Sulfure de fer(II) Synonymes sulfure de fer, sulfure ferreux, sulfure de fer noir No CAS No EINECS PubChem Apparence Solide gris anthracite à noir d'aspect métallique à cristaux plats ou en forme de bâtonnets Propriétés chimiques Formule brute FeS Masse molaire[1] 87,91 ± 0,007 g·mol-1
Fe 63,53 %, S 36,48 %,Propriétés physiques T° fusion 1 195 °C [2] Solubilité quasiment insoluble Masse volumique 4,84 g·cm-3 (20 °C)[2] Thermochimie S0solide 60,3 J·K-1·mol-1 à 25 °C [3] ΔfH0solide -100,0 kJ·mol-1 à 25 °C [3] ΔfusH° 31,5 kJ·mol-1 à 1 188 °C [3] Cp 50,5 J·K-1·mol-1 (25 °C, cristaux)[3] Cristallographie Structure type NiAs[4] Unités du SI & CNTP, sauf indication contraire. Le sulfure de fer(II), encore appelé sulfure ferreux, est le composé chimique de formule FeS. A l'instar de l'oxyde de fer(II), c'est un composé non-stœchiométrique. Il est pyrophorique (s'enflamme spontanément dans l'air) à l'état pulvérulent.
Sommaire
Différents sulfures de fer
Il existe plusieurs variétés de sulfures fer, qui diffèrent les unes des autres par leur stœchiométrie et leurs propriétés[5], présentant certaines analogies avec les oxydes correspondants :
- la pyrrhotite, un minéral ferromagnétique, comme le fer, de formule Fe1-xS crystallisant dans le système monoclinique.
- la troilite, une variété stœchiométrique de pyrrhotite, de formule FeS, ayant une symétrie hexagonale
- la mackinawite, le moins stable des sulfures de fer, avec une structure en couches de formule Fe1+xS
- la pyrite et la marcassite, des minéraux diamagnétiques de formule FeS2
- la greigite, un sulfure de fer(II,III) de formule Fe3S4 analogue à la magnétite Fe3O4 quant à ses propriétés ferromagnétiques.
Le sulfure de fer(III), de formule Fe2S3, est plutôt instable et tend à se dissocier en soufre et sulfure de fer(II).
Réactions chimiques
En laboratoire, on peut obtenir le sulfure de fer(II) en faisant réagir directement le fer et le soufre élémentaires, dans une réaction exothermique :
Le sulfure de fer(II) réagit avec l'acide chlorhydrique en donnant du chlorure de fer(II) et du sulfure d'hydrogène :
Biochimie et biologie
En environnement hypoxique, les bactéries sulfato-réductrices peuvent dégrader la matière organique en l'oxydant à l'aide des sulfates dissous dans l'eau, ce qui libère du sulfure d'hydrogène susceptible de réagir avec les ions métalliques dissous pour produire des sulfures métalliques insolubles ; ces composés, tels que le sulfure de fer(II), sont souvent bruns ou noirs, conférant une couleur sombre à l'environnement où ils se déposent.
La présence d'un précipité noir de sulfure de fer(II) dans un milieu de culture riche en fer (agar-agar, fer et peptone) permet de repérer les microorganismes qui métabolisent la cystéine à l'aide de la cystéine désulfhydrase, une enzyme qui libère du sulfure d'hydrogène, lequel réagit avec le citrate de fer pour former du sulfure de fer(II).
La même réaction entre H2S et fer se produit lors de la cuisson des œufs durs, à l'interface entre le jaune et le blanc : le fer du jaune s'oxyde au contact du sulfure d'hydrogène libéré par la cuisson du blanc pour former une couche brunâtre de sulfure de fer(II) au contact entre les deux parties de l'œuf[6].
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Entrée de « Iron(II) sulfide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 1 mai 2010 (JavaScript nécessaire)
- « Ferrous sulfide » dans la base de données Hazardous Substances Data Bank, consulté le 1 mai 2010
- (en) Bodie E. Douglas, Shih-Ming Ho, Structure and Chemistry of Crystalline Solids, Pittsburgh, PA, USA, Springer Science + Business Media, Inc., 2006, 346 p. (ISBN 0-387-26147-8), p. 64
- D. Vaughan, J. Craig, Mineral Chemistry of Metal Sulfides, Cambridge University Press, 1978. (ISBN 0-521-21489-0)
- (en) The Formation Of Ferrous Sulfide In Cooked Eggs
Catégories :- Composé du fer
- Sulfure
Wikimedia Foundation. 2010.
