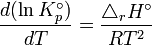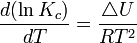Isochore de Van't Hoff
- Isochore de Van't Hoff
-
Relation de Van't Hoff
La relation de Van't Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d'équilibre d'une réaction chimique à l'énergie mise en jeu lors de cette réaction : enthalpie dans les cas isobares et énergie interne dans les cas isochores. Elle tire son nom du chimiste et physicien néerlandais Jacobus Henricus van 't Hoff.
Relation isobare
On donne le nom d'isobare de Van't Hoff à la formule suivante :
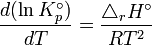
Relation isochore
On donne le nom d'isochore de Van't Hoff à la formule suivante :
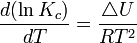
 Portail de la chimie
Portail de la chimie Portail de la physique
Portail de la physique
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article Isochore de Van't Hoff de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
Relation Isochore de Van't Hoff — Relation de Van t Hoff La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction :… … Wikipédia en Français
Relation isochore de van't hoff — Relation de Van t Hoff La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction :… … Wikipédia en Français
Van 't Hoff — may refer to:*Jacobus Henricus van t Hoff (1852 1911), Dutch chemist:*Van t Hoff factor, a ratio of solubility:*Van t Hoff equation (also known as the van t Hoff isochore), an equation that relates temperature change to enthalpy change *Robert… … Wikipedia
Isobare de Van't Hoff — Relation de Van t Hoff La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction :… … Wikipédia en Français
Relation de van 't Hoff — La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction : enthalpie dans les cas… … Wikipédia en Français
Relation de Van't Hoff — La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction : enthalpie dans les cas… … Wikipédia en Français
Van 't Hoff equation — The van t Hoff equation (also known as the van t Hoff isochore) in chemical thermodynamics relates the change in temperature ( T ) to the change in the equilibrium constant ( K ) given the standard enthalpy change ( ΔHo ) for the process. The… … Wikipedia
Relation Isobare de Van't Hoff — Relation de Van t Hoff La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction :… … Wikipédia en Français
Relation isobare de van't hoff — Relation de Van t Hoff La relation de Van t Hoff est une équation thermodynamique reliant la variation en fonction de la température de la constante d équilibre d une réaction chimique à l énergie mise en jeu lors de cette réaction :… … Wikipédia en Français
isochore — [ izɔkɔr ] adj. • 1948; de iso et gr. khôra « espace » ♦ Phys. À volume constant. Transformation isochore. ● isochore adjectif (du grec khôra, espace) Se dit d une transformation thermodynamique au cours de laquelle le volume reste constant.… … Encyclopédie Universelle
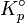 Constante d'équilibre relative aux pressions partielles.
Constante d'équilibre relative aux pressions partielles.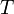 Température.
Température.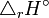 Enthalpie de réaction standard.
Enthalpie de réaction standard.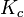 Constante d'équilibre relative aux concentrations molaires.
Constante d'équilibre relative aux concentrations molaires.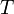 Température.
Température.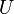 Énergie interne.
Énergie interne.