- XeF2
-
Difluorure de xénon
Difluorure de xénon 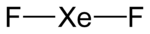
Structure du difluorure de xénon Général No CAS No EINECS SMILES InChI Propriétés chimiques Formule brute XeF2 Masse molaire 169,29 g∙mol-1
F 22,44 %, Xe 77,55 %,Propriétés physiques T° fusion 114 °C (sublimation) T° ébullition 114 °C Solubilité Décomposition avec l'eau Masse volumique 4 320 kg/m3 à 15 °C Unités du SI & CNTP, sauf indication contraire. Le difluorure de xénon est le composé chimique de formule XeF2. Il se présente sous forme d'un solide cristallin incolore qui se sublime à 114 °C. On l'obtient à partir de xénon et de fluor sous l'effet de la chaleur, d'un arc électrique ou d'un rayonnement ultraviolet :
- Xe + F2 + hν → XeF2.
Cette réaction est très facile et peut même être réalisée à la lumière du jour par temps couvert en laissant réagir du xénon avec du fluor.
XeF2 se décompose néanmoins après coup sous l'effet de la lumière ainsi qu'au contact de l'eau :
- 2 XeF2 + 2 H2O → 2 Xe + 4 HF + O2
C'est un agent fluorant efficace qui trouve de nombreuses applications car il n'introduit pas d'impuretés : le xénon libéré s'évacue simplement sous forme gazeuse. L'une d'entre elle intervient dans la fabrications des microsystèmes électromécaniques en faisant intervenir le difluorure de xénon pour graver le silicium. La molécule est adsorbée sur la pièce à graver et, au contact du silicium, se décompose en xénon et fluor ; ce dernier attaque le silicium en produisant du tétrafluorure de silicium :
- 2 XeF2 + Si → 2 Xe + SiF4
Le difluorure de xénon permet une gravure efficace et en profondeur sans recourir à des procédés énergétiques dispendieux tels que le bombardement ionique pour aboutir au même résultat.
La molécule XeF2 est un exemple traditionnel de molécule hypervalente avec une liaison à trois centres et quatre électrons : les orbitales atomiques p de trois atomes colinéaires s'organisent en trois orbitales moléculaires selon le schéma :
On observe :
-
- une orbitale moléculaire liante Ψ1 occupée,
- une orbitale moléculaire non liante Ψ2 occupée,
- une orbitale moléculaire antiliante Ψ3 vacante.
Ce type de liaison est à l'œuvre pour tous les fluorures de xénon.
Référence
- Hoppe, R. ; Daehne, W. ; Mattauch, H. ; Roedder, K., « FLUORINATION OF XENON », dans Angew. Chem. Intern. Ed. Engl.; Vol: 1, vol. 1, 1962-11-01, p. 599 [lien DOI]
Articles connexes
- Portail de la chimie
Catégories : Composé du fluor | Composé du xénon
Wikimedia Foundation. 2010.

